Hexafluoreto de selênio: diferenças entre revisões
Criado ao traduzir a página "Selenium hexafluoride" |
Correções, colocação de caixa infográfica. Etiquetas: Inserção de predefinição obsoleta Editor Visual |
||
| Linha 1: | Linha 1: | ||
{{chembox |
|||
{{Chembox entry}} |
|||
| Verifiedfields = changed |
|||
| Watchedfields = changed |
|||
| verifiedrevid = 432484439 |
|||
| ImageFileL1 = Selenium-hexafluoride-2D.png |
|||
| ImageSizeL1 = |
|||
| ImageFileR1 = Selenium-hexafluoride-3D-balls.png |
|||
| ImageSizeR1 = |
|||
| IUPACName = Hexafluoreto de selênio |
|||
| OtherNames = Fluoreto de selênio (VI), Fluoreto de selênio |
|||
|Section1={{Chembox Identifiers |
|||
| CASNo_Ref = {{cascite|correct|??}} |
|||
| CASNo = 7783-79-1 |
|||
| PubChem = 24558 |
|||
| RTECS = VS9450000 |
|||
| ChemSpiderID_Ref = {{chemspidercite|changed|chemspider}} |
|||
| ChemSpiderID = 22964 |
|||
| InChIKey = LMDVZDMBPZVAIV-UHFFFAOYAP |
|||
| StdInChI_Ref = {{stdinchicite|changed|chemspider}} |
|||
| StdInChI = 1S/F6Se/c1-7(2,3,4,5)6 |
|||
| StdInChIKey_Ref = {{stdinchicite|changed|chemspider}} |
|||
| StdInChIKey = LMDVZDMBPZVAIV-UHFFFAOYSA-N |
|||
| SMILES = F[Se](F)(F)(F)(F)F |
|||
| InChI = 1S/F6Se/c1-7(2,3,4,5)6 |
|||
}} |
|||
|Section2={{Chembox Properties |
|||
| Formula = SeF<sub>6</sub> |
|||
| MolarMass = 192.9534 g/mol |
|||
| Appearance = gás incolor |
|||
| Density = 0.007887 g/cm<sup>3</sup><ref name=CRC>{{RubberBible86th}}</ref> |
|||
| MeltingPtC = -39 |
|||
| BoilingPtC = -34.5 |
|||
| BoilingPt_notes = sublimante |
|||
| Solubility = insolúvel |
|||
| RefractIndex = 1.895 |
|||
| VaporPressure = >1 atm (20°C)<ref name=PGCH/> |
|||
| MagSus = −51.0·10<sup>−6</sup> cm<sup>3</sup>/mol |
|||
}} |
|||
|Section3={{Chembox Structure |
|||
| CrystalStruct = [[Ortorrômbico]], [[Pearson symbol|oP28]] |
|||
| SpaceGroup = Pnma, No. 62 |
|||
| Coordination = octaedral (''O<sub>h</sub>'') |
|||
| Dipole = 0 |
|||
}} |
|||
|Section7={{Chembox Hazards |
|||
| MainHazards = tóxico, corrosivo |
|||
| FlashPt = |
|||
| NFPA-H = 3 |
|||
| NFPA-F = 0 |
|||
| NFPA-R = 0 |
|||
| AutoignitionPt = |
|||
| IDLH = 2 ppm<ref name=PGCH>{{PGCH|0551}}</ref> |
|||
| REL = TWA 0.05 ppm<ref name=PGCH/> |
|||
| PEL = TWA 0.05 ppm (0.4 mg/m<sup>3</sup>)<ref name=PGCH/> |
|||
| LCLo = 10 ppm (rat, 1 hr)<br/>10 ppm (mouse, 1 hr)<br/>10 ppm (guinea pig, 1 hr)<ref>{{IDLH|7783791|Selenium hexafluoride}}</ref> |
|||
}} |
|||
|Section4={{Chembox Thermochemistry |
|||
| DeltaHf = 1030 kJ/mol<ref name = "Wiberg&Holleman">{{ cite book |author1=Wiberg, E. |author2=Holleman, A. F. | title = Inorganic Chemistry | year = 2001 | publisher = Elsevier | isbn = 0-12-352651-5 }}</ref> |
|||
| DeltaHc = |
|||
| Entropy = |
|||
| HeatCapacity = |
|||
}} |
|||
}} |
|||
O '''hexafluoreto de selênio''' é o [[composto inorgânico]] com a [[Fórmula química|fórmula]] SeF<sub>6</sub> . É um gás incolor muito [[tóxico]] descrito como tendo um "odor repulsivo". <ref name="decompose">{{Citar web|url=http://www.cpcb.nic.in/divisionsofheadoffice/pci-ssi/MATERIAL_SAFETY-DATABASE/MSDS2008/558.pdf|titulo=Material Safety}}</ref> Não é amplamente encontrado e não possui aplicações comerciais. |
O '''hexafluoreto de selênio''' é o [[composto inorgânico]] com a [[Fórmula química|fórmula]] SeF<sub>6</sub> . É um gás incolor muito [[tóxico]] descrito como tendo um "odor repulsivo". <ref name="decompose">{{Citar web|url=http://www.cpcb.nic.in/divisionsofheadoffice/pci-ssi/MATERIAL_SAFETY-DATABASE/MSDS2008/558.pdf|titulo=Material Safety}}</ref> Não é amplamente encontrado e não possui aplicações comerciais. |
||
| Linha 10: | Linha 73: | ||
== Segurança == |
== Segurança == |
||
Embora o hexafluoreto de selênio seja bastante [[inerte]] e demore a hidrolisar, é tóxico mesmo em baixas concentrações, <ref name="toxic">{{Citar web|url=http://www.atsdr.cdc.gov/MMG/MMG.asp?id=1015&tid=215|titulo=Medical Management Guidelines for Selenium Hexafluoride (SeF<sub>6</sub>)|publicação=CDC ATSDR}}</ref> principalmente por uma exposição mais longa. Nos EUA, os padrões da [[Occupational Safety and Health Administration|OSHA]] e da [[ ACGIH |ACGIH]] para exposição ao hexafluoreto de selênio são de um limite superior de em média 0,05 ppm no ar em um turno de trabalho de oito horas. Além disso, o hexafluoreto de selênio é designado como produto químico IDLH com um limite máximo de exposição permitido de 2 ppm. <ref>[https://www.cdc.gov/niosh/idlh/7783791.html Documentation for Immediately Dangerous To Life or Health Concentrations (IDLHs)]</ref> |
Embora o hexafluoreto de selênio seja bastante [[inerte]] e demore a hidrolisar, é tóxico mesmo em baixas concentrações, <ref name="toxic">{{Citar web|url=http://www.atsdr.cdc.gov/MMG/MMG.asp?id=1015&tid=215|titulo=Medical Management Guidelines for Selenium Hexafluoride (SeF<sub>6</sub>)|publicação=CDC ATSDR}}</ref> principalmente por uma exposição mais longa. Nos EUA, os padrões da [[Occupational Safety and Health Administration|OSHA]] e da [[ ACGIH |ACGIH]] para exposição ao hexafluoreto de selênio são de um limite superior de em média 0,05 ppm no ar em um turno de trabalho de oito horas. Além disso, o hexafluoreto de selênio é designado como produto químico IDLH com um limite máximo de exposição permitido de 2 ppm. <ref>[https://www.cdc.gov/niosh/idlh/7783791.html Documentation for Immediately Dangerous To Life or Health Concentrations (IDLHs)]</ref>{{Referências}} |
||
== Referências == |
|||
{{Referências}} |
|||
== Links externos == |
== Links externos == |
||
Revisão das 13h38min de 29 de abril de 2020
| Hexafluoreto de selênio Alerta sobre risco à saúde | |
|---|---|
|
|
| Nome IUPAC | Hexafluoreto de selênio |
| Outros nomes | Fluoreto de selênio (VI), Fluoreto de selênio |
| Identificadores | |
| Número CAS | |
| PubChem | |
| ChemSpider | |
| Número RTECS | VS9450000 |
| SMILES |
|
| InChI | 1S/F6Se/c1-7(2,3,4,5)6
|
| Propriedades | |
| Fórmula molecular | SeF6 |
| Massa molar | 192.9534 g/mol |
| Aparência | gás incolor |
| Densidade | 0.007887 g/cm3[1] |
| Ponto de fusão |
-39 °C, 234 K, -38 °F |
| Ponto de ebulição |
-34.5 °C, 239 K, -30 °F |
| Solubilidade em água | insolúvel |
| Pressão de vapor | >1 atm (20°C)[2] |
| Susceptibilidade magnética | −51.0·10−6 cm3/mol |
| Índice de refracção (nD) | 1.895 |
| Estrutura | |
| Estrutura cristalina | Ortorrômbico, oP28 |
| Grupo de espaço | Pnma, No. 62 |
| Geometria de coordenação |
octaedral (Oh) |
| Momento dipolar | 0 |
| Termoquímica | |
| Entalpia padrão de formação ΔfH |
1030 kJ/mol[3] |
| Riscos associados | |
| Principais riscos associados |
tóxico, corrosivo |
| NFPA 704 | |
| EUA Limite de exposição permissível (PEL) |
TWA 0.05 ppm (0.4 mg/m3)[2] |
| Página de dados suplementares | |
| Estrutura e propriedades | n, εr, etc. |
| Dados termodinâmicos | Phase behaviour Solid, liquid, gas |
| Dados espectrais | UV, IV, RMN, EM |
| Exceto onde denotado, os dados referem-se a materiais sob condições normais de temperatura e pressão Referências e avisos gerais sobre esta caixa. Alerta sobre risco à saúde. | |
O hexafluoreto de selênio é o composto inorgânico com a fórmula SeF6 . É um gás incolor muito tóxico descrito como tendo um "odor repulsivo". [4] Não é amplamente encontrado e não possui aplicações comerciais.
Estrutura, preparação e reações
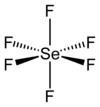
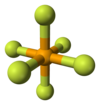
Como muitos compostos de selênio, o SeF6 é hipervalente. O composto possui geometria molecular octaédrica com um comprimento de ligação Se−F de 168,8 pm.
O SeF6 pode ser preparado a partir dos elementos [5] ou pela reação do trifluoreto de bromo (BrF3) com dióxido de selênio. O produto bruto é purificado por sublimação.
A reatividade relativa dos hexafluoretos de S, Se e Te segue a ordem TeF6 > SeF6 > SF6, sendo este último completamente inerte à hidrólise até altas temperaturas. O SeF6 também é resiste à hidrólise. O gás pode ser passado através de NaOH ou KOH a 10% sem alteração, mas reage com amônia gasosa a 200 °C. [6]
Segurança
Embora o hexafluoreto de selênio seja bastante inerte e demore a hidrolisar, é tóxico mesmo em baixas concentrações, [7] principalmente por uma exposição mais longa. Nos EUA, os padrões da OSHA e da ACGIH para exposição ao hexafluoreto de selênio são de um limite superior de em média 0,05 ppm no ar em um turno de trabalho de oito horas. Além disso, o hexafluoreto de selênio é designado como produto químico IDLH com um limite máximo de exposição permitido de 2 ppm. [8]
Referências
- ↑ Lide, D. R., ed. (2005). CRC Handbook of Chemistry and Physics 86th ed. Boca Raton (FL): CRC Press. ISBN 0-8493-0486-5
- ↑ a b Erro de citação: Etiqueta
<ref>inválida; não foi fornecido texto para as refs de nomePGCH - ↑ Wiberg, E.; Holleman, A. F. (2001). Inorganic Chemistry. [S.l.]: Elsevier. ISBN 0-12-352651-5
- ↑ «Material Safety» (PDF)
- ↑ «Sulfur, Selenium, and Tellurium Hexafluorides». Inorganic Syntheses. 1: 121–122. 1939. doi:10.1002/9780470132326.ch44
- ↑ Bonmann, S. (1994). King, R. B., ed. Encyclopedia of Inorganic Chemistry. John Wiley & Sons. ISBN 0-471-93620-0 Faltam os
|sobrenomes1=em Authors list (ajuda) - ↑ «Medical Management Guidelines for Selenium Hexafluoride (SeF6)». CDC ATSDR
- ↑ Documentation for Immediately Dangerous To Life or Health Concentrations (IDLHs)

