Intrão
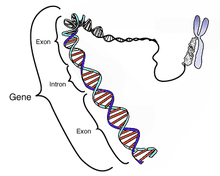
Intrões (português europeu) ou Introns (português brasileiro) são secções de DNA localizadas em um gene que são removidas por splicing de RNA durante a produção do mRNA ou de outro RNA funcional. São também chamados de sequências intervenientes (IVS) ou sequências interpostas.[1] Em outras palavras, os íntrões são regiões não-codificantes que são eliminadas por splicing antes da tradução.[2][3] A palavra íntrão é derivada do termo região intragênica (do inglês, "intragenic regions")[4], ou seja, corresponde a uma região dentro de um gene. O termo íntrão refere-se tanto à sequência de DNA dentro de um gene, quanto à sequência correspondente em transcritos de RNA. As sequências que são unidas no RNA maduro final após o splicing do RNA são exões.[5]
Inicialmente, os intrões eram considerados parte do DNA-lixo, por serem regiões não-codificantes de proteínas; no entanto, pesquisas posteriores demonstraram o papel dos intrões na regulação da expressão gênica[6] e também em um processo chamado splicing alternativo. Os intrões são encontrados nos genes da maioria dos organismos e de muitos vírus, e podem estar localizados em uma ampla gama de genes, incluindo aqueles que produzem proteínas, RNA ribossômico (RNAr) e RNA de transferência (RNAt). Quando as proteínas são geradas a partir de genes contendo intrões, o splicing do RNA ocorre como parte da via de processamento do RNA que segue a transcrição e precede a tradução.[5]
Descoberta
[editar | editar código-fonte]Em 1977, Richard Roberts e Philip Sharp, trabalhando de forma independente, durante os estudos de replicação de adenovírus em cultura de células humanas, demonstraram que os genes poderiam ser descontínuos.[7] Em 1978, o bioquímico estadunidense Walter Gilbert cunhou o termo intron para se referir às sequências não codificantes do DNA.[8]
Distribuição
[editar | editar código-fonte]A frequência de intrões em diferentes genomas varia consideravelmente em todo o espectro de organismos biológicos. Por exemplo, intrões são muito comuns dentro do genoma nuclear de vertebrados com mandíbula (como humanos e ratos), onde os genes codificadores de proteínas quase sempre contêm vários intrões. Por outro lado, os intrões são raros dentro dos genes nucleares de alguns microrganismos eucarióticos, por exemplo, a levedura (Saccharomyces cerevisiae).[9] Em contraste, os genomas mitocondriais de vertebrados são totalmente desprovidos de intrões, enquanto os de microrganismos eucarióticos podem conter muitos intrões.[10]
O gene Drosophila Dhc7 contém um intrão de mais de 3,6 Mb, que leva três dias para ser transcrito.[11][12] Em contraste, o menor comprimento de um intrão eucariótico conhecido possui 30 pares de bases, pertencendo ao gene humano MST1L.[13]
Classificação
[editar | editar código-fonte]Existem pelo menos quatro classes principais de intrões:[14][15]
- Íntrões auto-splicing do grupo I que são removidos por catálise de RNA
- Íntrões auto-splicing do grupo II que são removidos por catálise de RNA
- Íntrões em genes de RNA de transferência nuclear e de arqueias que são removidos por proteínas (intrões de RNAt)
- Íntrões em genes que codificam proteínas nucleares que são removidos por spliceossomos (intrões spliceossômicos)
Os intrões do grupo III são propostos como uma quinta família, mas pouco se sabe sobre o aparato bioquímico que medeia seu splicing. Eles parecem estar relacionados aos intrões do grupo II e, possivelmente, aos intrões spliceossômicos.
Íntrões do grupo I e II
[editar | editar código-fonte]intrões do grupo I e II são encontrados em genes codificadores de proteínas (RNA mensageiro), RNA de transferência e RNA ribossômico, em uma gama muito ampla entre os organismos vivos.[16] Após a transcrição em RNA, os íntrons do grupo I e do grupo II também realizam extensas interações internas que permitem que eles se dobrem em uma arquitetura tridimensional complexa e específica. Essas arquiteturas complexas permitem que alguns intrões do grupo I e do grupo II sejam auto-splicing, ou seja, a molécula de RNA que contém o intrões pode reorganizar sua própria estrutura covalente de modo a remover com precisão o intrões e ligar os exons na ordem correta. Em alguns casos, proteínas de ligação a intrões específicas estão envolvidas no splicing, auxiliando o intron a dobrar-se na estrutura tridimensional necessária para a atividade de self-splicing. Os intrões do grupo I e do grupo II são diferenciados por diferentes conjuntos de sequências conservadas internas e estruturas dobradas, e pelo fato de que o splicing de moléculas de RNA contendo íntrons do grupo II gera íntrons ramificados (como aqueles de RNAs spliceossômicos), enquanto os íntrons do grupo I usam um nucleotídeo de guanosina não codificado (tipicamente GTP) para iniciar o splicing, adicionando-o à extremidade 5' do intrões excisado.
Íntrões de RNAt
[editar | editar código-fonte]Os intrões de RNA de transferência que dependem de proteínas para remoção ocorrem em um local específico dentro da alça anticódon de precursores de tRNA não duplicados e são removidos por uma endonuclease de splicing de tRNA. Os exons são então ligados por uma segunda proteína, a ligase de splicing do tRNA.[17] Observe que os intrões autossplicáveis às vezes também são encontrados nos genes de RNAt.[18]
Íntrões spliceossômicos
[editar | editar código-fonte]Os intrões do pré-RNAm nuclear (intrões spliceossômicos) são caracterizados por sequências de intrões específicas localizadas nos limites entre os intrões e os exons.[19] Essas sequências são reconhecidas por moléculas de RNA spliceosomal quando as reações de splicing são iniciadas.[20] Além disso, eles contêm um ponto de ramificação, uma sequência de nucleotídeos particular perto da extremidade 3' do intrão, que se liga covalentemente à extremidade 5' do intrão durante o processo de splicing, gerando um intron ramificado (lariat). Além desses três elementos curtos conservados, as sequências do intrão do pré-RNAm nuclear são altamente variáveis. Os íntrons pré-RNAm nucleares são frequentemente muito mais longos do que os exons circundantes.
Funções biológicas e evolução
[editar | editar código-fonte]Embora os intrões não codifiquem produtos proteicos, eles são essenciais para a regulação da expressão gênica. Alguns intrões codificam RNAs funcionais por meio de processamento posterior após o splicing para gerar moléculas de RNA não-codificante.[21] O splicing alternativo é amplamente usado para gerar várias proteínas de um único gene. Além disso, alguns intrões desempenham papéis essenciais em uma ampla gama de funções regulatórias de expressão gênica.[22][23]
As origens biológicas dos intrões são obscuras. Após a descoberta inicial de intrões em genes codificadores de proteínas do núcleo eucariótico, houve um debate significativo sobre a origem dos intrões. A primeira hipótese afirma que os intrões foram herdados de um ancestral em comum entre os eucariotos e procariotos, e teria sido posteriormente perdido em procariotos. A segunda hipótese assume que os intrões teriam surgido recentemente no processo evolutivo. Outra teoria é que o spliceossomo e a estrutura íntron-exon dos genes é uma relíquia do mundo de RNA.[24] Ainda há um debate considerável sobre até que ponto essas hipóteses são mais corretas. O consenso popular no momento é que os intrões surgiram dentro da linhagem dos eucariotos como elementos egoístas.[25]
Referências
- ↑ «Descritores em Ciências da Saúde: DeCS». São Paulo: BIREME/OPAS/OMS. 2017. Consultado em 21 de outubro de 2020
- ↑ Ghosh, Shampa; Sinha, Jitendra Kumar (2017). Vonk, Jennifer; Shackelford, Todd, eds. «Intron». Springer International Publishing. Encyclopedia of Animal Cognition and Behavior (em inglês): 1–5. ISBN 978-3-319-47829-6. doi:10.1007/978-3-319-47829-6_70-1
- ↑ Editors B. D. «Intron». Biology Dictionary (em inglês). 2017-08-06
- ↑ Lopes, Sônia (2004). Bio: volume único. [S.l.]: Editora Saraiva. ISBN 8502047965
- ↑ a b Lewin Benjamin (1987). Genes 3 ed. New York: [s.n.] pp. 159–179, 386. ISBN 0-471-83278-2. OCLC 14069165
- ↑ Cohen, Jon (2010). Almost Chimpanzee. Searching for What Makes us Human, in Rainforests, Labs, Sanctuaries, and Zoos (em inglês). New York: Times Books. p. 24-26. 369 páginas. ISBN 978-0-8050-8307-1)
- ↑ Voet, D.; Voet, J.G.; Pratt, C.W. (2014). Fundamentos de Bioquímica - 4.ed.: A Vida em Nível Molecular. [S.l.]: Artmed Editora. ISBN 978-85-8271-066-1
- ↑ Gilbert, Walter (fevereiro de 1978). «Why genes in pieces?». Nature. 271 (5645): 501–501. ISSN 0028-0836. doi:10.1038/271501a0. Consultado em 21 de outubro de 2020
- ↑ Stajich, Jason E; Dietrich, Fred S; Roy, Scott W (2007). «Comparative genomic analysis of fungal genomes reveals intron-rich ancestors». Genome Biology. 8 (10): –223. ISSN 1465-6906. doi:10.1186/gb-2007-8-10-r223. Consultado em 22 de outubro de 2020
- ↑ Taanman, Jan-Willem (fevereiro de 1999). «The mitochondrial genome: structure, transcription, translation and replication». Biochimica et Biophysica Acta (BBA) - Bioenergetics. 1410 (2): 103–123. ISSN 0005-2728. doi:10.1016/S0005-2728(98)00161-3. Consultado em 22 de outubro de 2020
- ↑ Tollervey, David; Caceres, Javier F (novembro de 2000). «RNA Processing Marches on». Cell. 103 (5): 703–709. ISSN 0092-8674. doi:10.1016/S0092-8674(00)00174-4. Consultado em 22 de outubro de 2020
- ↑ Reugels, Alexander M.; Kurek, Roman; Lammermann, Ulrich; Bünemann, Hans (2000). «Mega-introns in the Dynein Gene DhDhc7(Y) on the Heterochromatic Y Chromosome Give Rise to the Giant Threads Loops in Primary Spermatocytes of Drosophila hydei». Genetics. 154 (2): 759–769. ISSN 0016-6731
- ↑ Piovesan, Allison; Caracausi, Maria; Ricci, Marco; Strippoli, Pierluigi; Vitale, Lorenza; Pelleri, Maria Chiara (dezembro de 2015). «Identification of minimal eukaryotic introns through GeneBase, a user-friendly tool for parsing the NCBI Gene databank». DNA Research. 22 (6): 495–503. ISSN 1340-2838. doi:10.1093/dnares/dsv028. Consultado em 22 de outubro de 2020
- ↑ Haugen, Peik; Simon, Dawn M; Bhattacharya, Debashish (2005). «The natural history of group I introns». TRENDS in Genetics. 21 (2): 111–119
- ↑ Alberts, B. (2017). Biologia Molecular Da Célula. [S.l.]: ARTMED. ISBN 978-85-8271-422-5
- ↑ Cech, T. R. (1990). «Self-splicing of group I introns». Annual Review of Biochemistry. 59: 543–568. ISSN 0066-4154. PMID 2197983. doi:10.1146/annurev.bi.59.070190.002551
- ↑ Greer, C. L.; Peebles, C. L.; Gegenheimer, P.; Abelson, J. (fevereiro de 1983). «Mechanism of action of a yeast RNA ligase in tRNA splicing». Cell. 32 (2): 537–546. ISSN 0092-8674. PMID 6297798. doi:10.1016/0092-8674(83)90473-7
- ↑ Reinhold-Hurek, B.; Shub, D. A. (14 de maio de 1992). «Self-splicing introns in tRNA genes of widely divergent bacteria». Nature. 357 (6374): 173–176. ISSN 0028-0836. PMID 1579169. doi:10.1038/357173a0
- ↑ Padgett, R. A.; Grabowski, P. J.; Konarska, M. M.; Seiler, S.; Sharp, P. A. (1986). «Splicing of messenger RNA precursors». Annual Review of Biochemistry. 55: 1119–1150. ISSN 0066-4154. PMID 2943217. doi:10.1146/annurev.bi.55.070186.005351
- ↑ Guthrie, C; Patterson, B (dezembro de 1988). «Spliceosomal SNRNAS». Annual Review of Genetics. 22 (1): 387–419. ISSN 0066-4197. doi:10.1146/annurev.ge.22.120188.002131. Consultado em 22 de outubro de 2020
- ↑ Rearick D, Prakash A, McSweeny A, Shepard SS, Fedorova L, Fedorov A (março 2011). «Critical association of ncRNA with introns». Nucleic Acids Res. 39 (6): 2357–66. PMC 3064772
 . PMID 21071396. doi:10.1093/nar/gkq1080
. PMID 21071396. doi:10.1093/nar/gkq1080
- ↑ Bicknell AA, Cenik C, Chua HN, Roth FP, Moore MJ (dezembro 2012). «Introns in UTRs: why we should stop ignoring them.». BioEssays. 34 (12): 1025–34. PMID 23108796. doi:10.1002/bies.201200073
- ↑ Cenik, Can; Chua, Hon Nian; Zhang, Hui; Tarnawsky, Stefan P.; Akef, Abdalla; Derti, Adnan; Tasan, Murat; Moore, Melissa J.; Palazzo, Alexander F.; Roth, Frederick P. (2011). Snyder, Michael, ed. «Genome Analysis Reveals Interplay between 5′UTR Introns and Nuclear mRNA Export for Secretory and Mitochondrial Genes». PLOS Genetics. 7 (4): e1001366. ISSN 1553-7404. PMC 3077370
 . PMID 21533221. doi:10.1371/journal.pgen.1001366
. PMID 21533221. doi:10.1371/journal.pgen.1001366
- ↑ Penny D, Hoeppner MP, Poole AM, Jeffares DC (novembro 2009). «An overview of the introns-first theory». Journal of Molecular Evolution. 69 (5): 527–40. Bibcode:2009JMolE..69..527P. PMID 19777149. doi:10.1007/s00239-009-9279-5
- ↑ Cavalier-Smith, T (1985). «Selfish DNA and the origin of introns.». Nature. 315 (6017): 283–4. Bibcode:1985Natur.315..283C. PMID 2987701. doi:10.1038/315283b0
