Quiralidade (química)
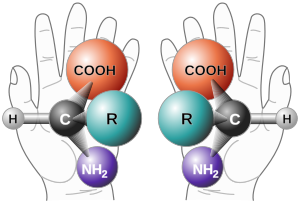

Em química, uma molécula ou íon é chamado quiral se não puder ser sobreposto em sua imagem especular por qualquer combinação de rotações, translações e algumas mudanças conformacionais. Essa propriedade geométrica é chamada de quiralidade. Os termos são derivados do grego antigo χείρ (mão); que é o exemplo canônico de um objeto com essa propriedade.
Esteroisômeros são moléculas ou íons que possuem a mesma conectividade, porém com arranjos espaciais diferentes. Já o enantiômero se caracteriza por estereoisômeros que são imagens de espelho (ou especular) e não são sobreponíveis[1]; eles são freqüentemente distinguidos como "destros" ou "canhotos" por sua configuração absoluta ou algum outro critério. Os dois enantiômeros têm as mesmas propriedades químicas, exceto quando reagem com outros compostos quirais. Eles também têm as mesmas propriedades físicas, exceto que muitas vezes têm atividades ópticas opostas. Uma mistura homogênea dos dois enantiômeros em partes iguais é chamada de racêmica e geralmente difere química e fisicamente dos enantiômeros puros.[2][3][4]
As moléculas quirais geralmente têm um elemento estereogênico do qual surge a quiralidade. O tipo mais comum de elemento estereogênico é um centro estereogênico, ou estereocentro. No caso de compostos orgânicos, os estereocentros mais frequentemente assumem a forma de um átomo de carbono com quatro grupos distintos ligados a ele em uma geometria tetraédrica. Um dado estereocentro tem duas configurações possíveis, que dão origem a estereoisômeros (diastereômeros e enantiômeros) em moléculas com um ou mais estereocentros. Os diastereoisômeros são estereoisômeros que não são imagem especular e não são sobreponíveis. [5]Para uma molécula quiral com um ou mais estereocentros, o enantiômero corresponde ao estereoisômero em que cada estereocentro tem a configuração oposta. Um composto orgânico com apenas um carbono estereogênico é sempre quiral. Por outro lado, um composto orgânico com múltiplos carbonos estereogênicos é tipicamente, mas nem sempre, quiral. Em particular, se os estereocentros estiverem configurados de tal forma que a molécula tenha um plano interno de simetria, então a molécula é aquiral e é conhecida como um composto meso. Menos comumente, outros átomos como N, P, S e Si também podem servir como estereocentros, desde que tenham quatro substituintes distintos (incluindo pares de elétrons livres) ligados a eles.
Moléculas com quiralidade provenientes de um ou mais estereocentros são classificadas como possuindo quiralidade central. Existem dois outros tipos de elementos estereogênicos que podem dar origem à quiralidade, um eixo estereogênico (quiralidade axial) e um plano estereogênico (quiralidade planar). Finalmente, a curvatura inerente de uma molécula também pode dar origem à quiralidade (quiralidade inerente). Esses tipos de quiralidade são muito menos comuns do que a quiralidade central. BINOL é um exemplo típico de uma molécula axial quiral, enquanto o trans-cicloocteno é um exemplo comumente citado de uma molécula quiral planar. Finalmente, o heliceno possui quiralidade helicoidal, que é um tipo de quiralidade inerente.
A quiralidade é um conceito importante para estereoquímica e bioquímica. A maioria das substâncias relevantes para a biologia são quirais, como carboidratos ( açúcares, amido e celulose ), os aminoácidos que são os blocos de construção das proteínas e os ácidos nucleicos. Em organismos vivos, normalmente encontramos apenas um dos dois enantiômeros de um composto quiral. Por essa razão, os organismos que consomem um composto quiral geralmente podem metabolizar apenas um de seus enantiômeros. Pela mesma razão, os dois enantiômeros de um produto farmacêutico quiral geralmente têm potências ou efeitos.[2][3][4]
Ver também
[editar | editar código-fonte]Referências
- ↑ Química Orgânica I (PDF). [S.l.: s.n.]
- ↑ a b Clayden, Jonathan; Greeves, Nick; Warren, Stuart (2012). Organic Chemistry (2nd ed.). Oxford, UK: Oxford University Press. pp. 319f, 432, 604np, 653, 746int, 803ketals, 839, 846f. ISBN 978-0199270293
- ↑ a b Eliel, Ernest Ludwig; Wilen, Samuel H.; Mander, Lewis N. (1994). "Chirality in Molecules Devoid of Chiral Centers (Chapter 14)". Stereochemistry of Organic Compounds. Chirality. Vol. 9 (1st ed.). New York, NY, USA: Wiley & Sons. pp. 428–430. doi:10.1002/(SICI)1520-636X(1997)9:5/6<428::AID-CHIR5>3.0.CO;2-1. ISBN 978-0471016700
- ↑ a b Gal, Joseph (2013). "Molecular Chirality: Language, History, and Significance". Differentiation of Enantiomers I. Chirality. Topics in Current Chemistry. Vol. 340. pp. 1–20. doi:10.1007/128_2013_435. ISBN 978-3-319-03238-2
- ↑ Química Orgânica I (PDF). [S.l.: s.n.]
