Citocalasina
Citocalasina é uma substância inibidora da polimerização de filamentos de actina, análoga à colchicina, mas que actua sobre proteínas diferentes. As citocalasinas são metabolitos fúngicos que apresentam a propriedade de se ligarem aos filamentos de actina e bloquearem a sua polimerização e alongamento.[1] A citocalasina ocorre em diferentes formas, com pequenas diferenças na sua estrutura química, designadas por citocalasinas A a J.
Descrição
[editar | editar código-fonte]Como resultado da inibição da polimerização da actina, as citocalasinas podem alterar a morfologia celular, inibir processos celulares como a divisão celular e até mesmo induzir as células a sofrer apoptose.[1] As citocalasinas apresentam a capacidade de permear as membranas celulares, impedir a translocação celular e levar as células a enuclear.[2]
As citocalasinas podem também afectar alguns processos biológicos não relacionados com polimerização da actina. Por exemplo, a citocalasina A e a citocalasina B podem inibir o transporte de monossacarídeos através da membrana celular,[2] foi descoberto que a citocalasina H participa no processo de regulação do crescimento das plantas,[3] a citocalasina D inibe a síntese de proteinas[4] e a citocalasina E impede a angiogénese.[5]
Sabe-se que as citoqualasinas se ligam às extremidades farpadas e de crescimento rápido dos microfilamentos, o que causa o bloqueio da montagem e desmontagem de monómeros individuais de actina a partir da extremidade a que estejam ligadas. Uma vez ligadas, as citocalasinas isolam a extremidade do filamento de actina, inactivando a sua acção. Cada molécula de citocalasina liga-se a um único filamento de actina.[2]
Estudos realizados com citocalasina D (CD) descobriram que a formação de dímeros de CD-actina envolve a presença de actina ligada a ATP.[6] Estes dímeros de CD-actina são reduzidos a monómeros de CD-actina em resultado da hidrólise da molécual de ATP. O monómero CD-actina resultante pode ligar-se ao monómero ATP-actina para voltar a formar o dímero CD-actina.[2]
Na sua acção bioquímica, CD é extremamente eficiente, pois apenas são necessárias muito baixas concentrações (0.2 μM) para impedir o enrugar da membrana e interromper o processo de reacção em esteira (ou treadmilling).[7]
Os efeitos de diversas citocalasinas nos filamentos de actina foram analisados, tendo-se concluído que concentrações mais altas (2-20 μM) de CD eram necessárias para remover as fibras de tensão do citoesqueleto.[7]
Em contraste, a latrunculina inibe a polimerização dos filamentos de actina ligando-se aos monómeros da actina.
Usos e aplicações das citocalasinas
[editar | editar código-fonte]Os microfilamentos de actina foram amplamente estudados usando citocalasinas. Devido à sua natureza química, os estudos da acção das citocalasinas podem contribuir para determinar a importância da actina em vários processos biológicos. O uso de citocalasinas permitiu aos investigadores entender melhor a polimerização da actina, a motilidade celular, o enrugamento das membranas (ruffling), a divisão celular e a contracção e a rigidez celular. O uso de citocalasinas tem sido tão importante para a compreensão do movimento do citoesqueleto e de muitos outros processos biológicos que os investigadores já criaram duas citocalasinas sintéticas.[1]
A citocalasina já encontrou aplicação prática em ensaios de tromboelastometria (TEM) do sangue total para a avaliação de distúrbios de fibrinogénio e polimerização de fibrina no ensaio FIBTEM na técnica ROTEM (rotational thromboelastometry ou tromboelastometria rotacional). Este teste baseia-se no princípio de que a citocalase D inibe muito eficazmente a função das plaquetas sanguíneas pela inibição dos elementos contráteis.[8]
A inibição plaquetária pelas citocalasinas é mais eficaz do que quando as plaquetas são bloqueadas com recurso a antagonistas dos receptores GPIIb/IIIa.[9] Testes in vitro e clínicos indicam que a intensidade da coagulação no FIBTEM aumenta de modo proporcional à concentração de fibrinogénio, independentemente da contagem de plaquetas,[10] pelo que a deficiência de fibrinogénio ou os distúrbios de polimerização da fibrina podem ser rapidamente detectados pelo teste.
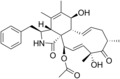
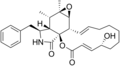
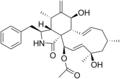
Estrutura química
[editar | editar código-fonte]As diferentes formas da citocalasina apresentam a seguinte estrutura química:
Ver também
[editar | editar código-fonte]Referências
[editar | editar código-fonte]- ↑ a b c Haidle, A. M.; Myers, A. G. (2004). «An Enantioselective, Modular, and General Route to the Cytochalasins: Synthesis of L-696,474 and Cytochalasin B» (pdf). Proceedings of the National Academy of Sciences. 101 (33): 12048–12053. PMC 514432
 . PMID 15208404. doi:10.1073/pnas.0402111101
. PMID 15208404. doi:10.1073/pnas.0402111101
- ↑ a b c d Cooper, J. A. (1987). «Effects of Cytochalasin and Phalloidin on Actin» (pdf). Journal of Cell Biology. 105 (4): 1473–1478. PMC 2114638
 . PMID 3312229. doi:10.1083/jcb.105.4.1473
. PMID 3312229. doi:10.1083/jcb.105.4.1473
- ↑ Cox, R. H.; Cutler, H. G.; Hurd, R. E.; Cole, R. J. (1983). «Proton and Carbon-13 Nuclear Magnetic Resonance Studies of the Conformation of Cytochalasin H Derivatives and Plant Growth Regulating Effects of Cytochalasins». Journal of Agricultural and Food Chemistry. 31 (2): 405–408. doi:10.1021/jf00116a055
- ↑ Ornelles, D. A.; Fey, E. G.; Penman, S. (1986). «Cytochalasin Releases mRNA from the Cytoskeletal Framework and Inhibits Protein Synthesis» (pdf). Molecular and Cellular Biology. 6 (5): 1650–1662. PMC 367692
 . PMID 3785175
. PMID 3785175
- ↑ Udagawa, T.; Yuan, J.; Panigrahy, D.; Chang, Y.-H.; Shah, J.; D’Amato, R. J. (2000). «Cytochalasin E, an Epoxide Containing Aspergillus-Derived Fungal Metabolite, Inhibits Angiogenesis and Tumor Growth» (pdf). Journal of Pharmacology and Experimental Therapeutics. 294 (2): 421–427. PMID 10900214
- ↑ Goddette, D. W.; Frieden, C. (1987). «Actin Polymerization - The Mechanism of Action of Cytochalasin D» (pdf). Journal of Biological Chemistry. 261 (34): 15974–15980. PMID 3023337
- ↑ a b Yahara, I.; Harada, F.; Sekita, S.; Yoshihira, K.; Natori, S. (1982). «Correlation between effects of 24 different cytochalasins on cellular structures and cellular events and those on actin in vitro» (pdf). Journal of Cell Biology. 92 (1): 69–78. PMC 2112011
 . PMID 7199054. doi:10.1083/jcb.92.1.69
. PMID 7199054. doi:10.1083/jcb.92.1.69
- ↑ May, J. A.; Ratan, H.; Glenn, J. R.; Lösche, W.; Spangenberg, P.; Heptinstall, S. (1998). «GPIIb-IIIa antagonists cause rapid disaggregation of platelets pretreated with cytochalasin D. Evidence that the stability of platelet aggregates depends on normal cytoskeletal assembly». Platelets. 9 (3–4): 227–232. PMID 16793707. doi:10.1080/09537109876744
- ↑ Lang, T.; Toller, W.; Gütl, M.; Mahla, E.; Metzler, H.; Rehak, P.; März, W.; Halwachs-Baumann, G. (2004). «Different effects of abciximab and cytochalasin D on clot strength in thrombelastography» (pdf). Journal of Thrombosis and Haemostasis. 2 (1): 147–153. PMID 14717978. doi:10.1111/j.1538-7836.2004.00555.x
- ↑ Lang, T.; Johanning, K.; Metzler, H.; Piepenbrock, S.; Solomon, C.; Rahe-Meyer, N.; Tanaka, K. A. (2009). «The effects of fibrinogen levels on thromboelastometric variables in the presence of thrombocytopenia» (pdf). Anesthesia and Analgesia. 108 (3): 751–758. PMID 19224779. doi:10.1213/ane.0b013e3181966675