Estrutura de Keggin



A estrutura de Keggin é a forma estrutural mais conhecida para heteropoliácidos. É a forma estrutural dos ânions α-Keggin, que têm uma fórmula geral de [XM
12O
40]n−, onde X é o heteroátomo (geralmente um elemento não-metálico do bloco p), dos quais os mais comuns são fósforo e arsênio pentavalentes (PV e AsV), silício tetravalente (SiIV) ou boro trivalente (BIII), M é o átomo do metal hospedeiro, o qual é chamado de adendo, sendo os mais comuns o molibdênio (Mo), tungstênio (W) e vanádio (V), e O representa os átomos de oxigênio.[1] A estrutura se automonta em solução aquosa ácida e é um tipo comumente usado de catalisadores de polioxometalato.
História
[editar | editar código-fonte]O primeiro composto contendo um ânion α-Keggin, fosfomolibdato de amônio ((NH
4)
3[PMo
12O
40]), foi relatado pela primeira vez por Berzelius em 1826. Em 1892, Blomstrand propôs a estrutura do ácido fosfomolíbdico (H
3[PMo
12O
40]) e outros poliácidos como uma configuração de cadeia ou anel. Alfred Werner, usando as ideias de compostos de coordenação de Copaux, tentou explicar a estrutura do ácido silicotúngstico. Ele assumiu um grupo central formado pelo íon SiO
44−, envolvido por quatro unidades [RW
2O
6]+, onde R é um íon monopositivo. Os grupos [RW
2O
6]+ estão ligados ao grupo central por valências primárias. Mais dois grupos [RW
2O
7] seriam ligados ao grupo central por valências secundárias. Esta proposta foi responsável pelas características da maioria dos poliácidos, mas não de todos. [carece de fontes]
Em 1928, Linus Pauling propôs uma estrutura para os ânions α-Keggin consistindo de um íon central tetraédrico, [XO
4]n−8, enjaulado por doze octaedros WO
6. Nesta estrutura proposta, três dos oxigênios em cada um dos octaedros compartilhavam elétrons com três octaedros vizinhos. Como resultado, 18 átomos de oxigênio foram usados como átomos de ponte entre os átomos de metal. Os átomos de oxigênio restantes se ligaram a um próton. Esta estrutura explicou muitas características que foram observadas, como basicidades de sais de metais alcalinos e a forma hidratada de alguns dos sais. No entanto, a estrutura não conseguiu explicar a estrutura de ácidos desidratados. [carece de fontes]
James Fargher Keggin com o uso de difração de raios X determinou experimentalmente a estrutura dos ânions α-Keggin em 1934. A estrutura Keggin é responsável pelos ânions α-Keggin hidratados e desidratados sem a necessidade de mudança estrutural significativa. A estrutura Keggin é a estrutura amplamente aceita para os ânions α-Keggin.[2]
Estrutura e Propriedades físicas
[editar | editar código-fonte]A estrutura tem simetria tetraédrica completa e é composta de um heteroátomo cercado por quatro átomos de oxigênio para formar um tetraedro. O heteroátomo está localizado centralmente e enjaulado por 12 unidades octaédricas MO
6 ligadas entre si pelos átomos de oxigênio vizinhos. Há um total de 24 átomos de oxigênio de ponte que ligam os 12 átomos de adendo. Os centros metálicos nos 12 octaedros estão dispostos em uma esfera quase equidistante um do outro, em quatro unidades M
3O
13, dando à estrutura completa uma simetria tetraédrica geral. O comprimento da ligação entre os átomos varia dependendo do heteroátomo (X) e dos átomos adendos (M). Para o ácido 12-fosfotúngstico, Keggin determinou que o comprimento de ligação entre o heteroátomo e cada um dos quatro átomos centrais de oxigênio é de 1,5 Å. O comprimento da ligação do oxigênio central aos átomos do adendo é de 2,43 Å. O comprimento da ligação entre os átomos de adendo e cada um dos oxigênios de ponte é de 1,9 Å. Os 12 átomos de oxigênio restantes, cada um duplamente ligado a um átomo de adendo, têm um comprimento de ligação de 1,70 Å. Os octaedros são, portanto, distorcidos.[3][4] Essa estrutura permite que a molécula hidrate e desidrate sem mudanças estruturais significativas e a molécula é termicamente estável no estado sólido para uso em reações de fase de vapor em altas temperaturas (400−500°C).[5]

Incluindo a estrutura original de Keggin, existem 5 isômeros , designados pelos prefixos α-, β-, γ-, δ- e ε-. A estrutura original de Keggin é designada α. Esses isômeros são às vezes denominados Baker, Baker–Figgis ou isômeros rotacionais,[6] Eles envolvem diferentes orientações rotacionais do unidades M
3O
13, o que diminui a simetria da estrutura geral.
Estruturas de Keggin Lacunárias
[editar | editar código-fonte]O termo lacunar é aplicado a íons que têm um fragmento faltando, às vezes chamados de estruturas defeituosas. Exemplos são os [XM
11O
39]n− e [XM
9O
34]n− formado pela remoção da estrutura de Keggin de átomos de M e O suficientes para eliminar 1 ou 3 átomos adjacentes de octaedros MO
6. A estrutura de Dawson é composta de dois fragmentos lacunares de Keggin com 3 octaedros faltantes.
Cátions do grupo 13 com estrutura de Keggin
[editar | editar código-fonte]O cátion cluster [Al
13O
4(OH)
24(H
2O)
12]7+ tem a estrutura de Keggin com um átomo de alumínio tetraédrico no centro do cluster coordenado a 4 átomos de oxigênio. A fórmula pode ser expressa como[AlO
4Al
12(OH)
24(H
2O)
12]7+.[7] Este íon é geralmente chamado de “íon Al
13". O análogo Ga
13''"; também é conhecido.[8][9]
O íon de ferro Keggin
[editar | editar código-fonte]Devido às químicas aquosas semelhantes de alumínio e ferro trivalente, há muito tempo se pensa que um policátion de ferro análogo deve ser isolável a partir dde uma solução aquosa. Além disso, em 2007, a estrutura da ferrihidrita foi determinada e mostrou ser construída de íons Keggin de ferro.[10] Isso capturou ainda mais a imaginação e o impulso dos cientistas para isolar o íon Keggin de ferro. Em 2015, o íon Keggin de ferro foi isolado da água, mas como um poliânion com carga −17; e era necessária uma química protetora.[11] A água ligada ao ferro é muito ácida; portanto, é difícil capturar a forma intermediária do íon Keggin sem ligantes volumosos e não próticos em vez da água encontrada no íon Keggin de alumínio. No entanto, mais importante nesta síntese foi o uso de contra-íons de bismuto (Bi3+), que forneceram alta carga positiva para estabilizar a alta carga negativa do poliânion heptadecavalente. [carece de fontes]
Propriedades químicas
[editar | editar código-fonte]A estabilidade da estrutura de Keggin permite que os metais no ânion sejam prontamente reduzidos sem grandes mudanças na estrutura. Dependendo do solvente, da acidez da solução e da carga do ânion α-Keggin, ele pode ser reduzido reversivelmente em etapas de um ou vários elétrons.[12] Por exemplo, o ânion silicotungstato pode ser reduzido a um estado de oxidação -20.[13] Alguns ânions, como o ácido silicotungstico, são fortes o suficiente como um ácido como o ácido sulfúrico e podem ser usados em seu lugar como um catalisador ácido. [carece de fontes]
Preparação
[editar | editar código-fonte]Em geral, os ânions α-Keggin são sintetizados em soluções ácidas. Por exemplo, o ácido 12-fosfotúngstico é formado pela condensação do íon fosfato com íons tungstato. O heteropoliácido que é formado tem a estrutura Keggin.[5]
- PO3–
4 + 12 WO2–
4 + 27 H+
→ H
3PW
12O
40 + 12 H
2O
Usos
[editar | editar código-fonte]Os ânions α-Keggin têm sido usados como catalisadores nas seguintes reações: hidratação, polimerização e reação de oxidação como catalisadores.[5] As empresas químicas japonesas comercializaram o uso dos compostos na hidratação de propeno, oxidação de metacroleína, hidratação de isobuteno e n-buteno e polimerização de THF.[14][15]
Estrutura de Dawson
[editar | editar código-fonte]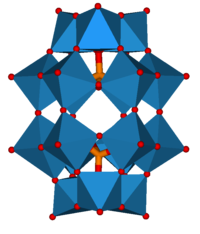
A estrutura de Dawson é um outro motivo estrutural bem conhecido para heteropoliácidos. A estrutura de Dawson pode ser vista como a fusão de duas estruturas de Keggin defeituosas, fragmentos com três octaedros faltantes. Como nas estruturas de Keggin, a estrutura de Dawson tem um oxiânion em seu núcleo. Ao contrário das estruturas de Keggin, existem dois desses ânions, um em cada lado do ânion elipsoidal. Um exemplo é [S
2W
18O
62]4−, que também pode ser descrito como [(SO
4)
2(WO
3)
18]4−.[16]
Comumente, as estruturas de Dawson apresentam fosfato como os oxiânions centrais . Quando o ânion Keggin [PW
12O
40]3– é deixado em solução aquosa, ele se converte em [P
2W
18O
62]6–.[17]
Referências
- ↑ Predefinição:Housecroft2nd
- ↑ Bailar, J. C. Jr. (1956). The Chemistry of the Coordination Compounds. [S.l.]: Reinhold Publishing. pp. 472–482
- ↑ Keggin, J. F.; Bragg, William Lawrence (1 de março de 1934). «The structure and formula of 12-phosphotungstic acid». Proceedings of the Royal Society of London. Series A, Containing Papers of a Mathematical and Physical Character. 144 (851): 75–100. Bibcode:1934RSPSA.144...75K. doi:10.1098/rspa.1934.0035
- ↑ Brown, G. M.; Noe-Spirlet, M.-R.; Busing, W. R.; Levy, H. A. (15 de abril de 1977). «Dodecatungstophosphoric acid hexahydrate, (H5O2+)3(PW12O403−). The true structure of Keggin's 'pentahydrate' from single-crystal X-ray and neutron diffraction data». Acta Crystallographica Section B: Structural Crystallography and Crystal Chemistry (em inglês). 33 (4): 1038–1046. Bibcode:1977AcCrB..33.1038B. ISSN 0567-7408. doi:10.1107/S0567740877005330
- ↑ a b c Izumi, Y.; Urabe, K.; Onaka, M. (1992). Zeolite, Clay, and Heteropoly Acid in Organic Reactions. Tokyo: Kodansha. pp. 100–105. ISBN 978-0-12-007841-7
- ↑ Baker, L. C. W.; Figgis, J. S. (1970). «A New Fundamental Type of Inorganic Complex: Hybrid between Heteropoly and Conventional Coordination Complexes. Possibilities for Geometrical Isomerisms in 11-, 12-, 17-, and 18-Heteropoly Derivatives». Journal of the American Chemical Society. 92 (12): 3794–3797. doi:10.1021/ja00715a047
- ↑ Verevkin, A.; Pearlman, A.; Slstrokysz, W.; Zhang, J.; Currie, M.; Korneev, A.; Chulkova, G.; Okunev, O.; Kouminov, P.; Smirnov, K.; Voronov, B.; N. Gol'tsman, G.; Sobolewski, Roman (2004). "Ultrafast superconducting single-photon detectors for near-infrared-wavelength quantum communications". Journal of Modern Optics 51 (12): 1447–1458. doi:10.1080/09500340410001670866.
- ↑ Bradley, S. M.; Kydd, R. A.; Yamdagni, R. (1990). «Detection of a new polymeric species formed through the hydrolysis of gallium(III) salt solutions». Journal of the Chemical Society, Dalton Transactions. 1990 (2): 413–417. doi:10.1039/DT9900000413
- ↑ Son, Jung-ho; Kwon, Young-uk (2003). «New Ionic Crystals of Oppositely Charged Cluster Ions and Their Characterization». Inorganic Chemistry. 42 (13): 4153–4159. PMID 12817975. doi:10.1021/ic0340377
- ↑ Michel, F. Marc; Ehm, Lars; Antao, Sytle M.; Lee, Peter L.; Chupas, Peter J.; Liu, Gang; Strongin, Daniel R.; Schoonen, Martin A. A.; Phillips, Brian L.; Parise, John B. (22 de junho de 2007). «The Structure of Ferrihydrite, a Nanocrystalline Material». Science (em inglês). 316 (5832): 1726–1729. Bibcode:2007Sci...316.1726M. ISSN 0036-8075. PMID 17525301. doi:10.1126/science.1142525
- ↑ Sadeghi, O.; Zakharov, L. N.; Nyman, M. (2015). «Aqueous formation and manipulation of the iron-oxo Keggin ion». Science. 347 (6228): 1359−1362. Bibcode:2015Sci...347.1359S. PMID 25721507. doi:10.1126/science.aaa4620
- ↑ Okuhara, T.; Mizuno, N.; Misono, M. (1996). Catalytic Chemistry of Heteropoly Compounds. Col: Advances in Cayalysis. 41. [S.l.]: Academic Press. pp. 191–193[Falta ISBN]
- ↑ Pope, M. T. (1983). Heteropoly and Isopolyoxometalates. Col: Inorganic Chemistry Concepts. 8. Heidelberg: Springer-Verlag. pp. 101–107[Falta ISBN]
- ↑ Pope, M. T.; Müller, A. (1994). Polyoxometalates: From Platonic Solids to Anti-Retroviral Activity. Netherlands: Kluwer Academic Publications. pp. 262–265[Falta ISBN]
- ↑ Barton, Thomas J.; Bull, Lucy M.; Klemperer, Walter G.; Loy, Douglas A.; McEnaney, Brian; Misono, Makoto; Monson, Peter A.; Pez, Guido; Scherer, George W.; Vartuli, James C.; Yaghi, Omar M. (1 de outubro de 1999). «Tailored Porous Materials». Chemistry of Materials. 11 (10): 2633–2656. ISSN 0897-4756. doi:10.1021/cm9805929
- ↑ Richardt, Peter J. S.; Gable, Robert W.; Bond, Alan M.; Wedd, Anthony G. (2001). «Synthesis and Redox Characterization of the Polyoxo Anion, γ*-[S2W18O62]4-: A Unique Fast Oxidation Pathway Determines the Characteristic Reversible Electrochemical Behavior of Polyoxometalate Anions in Acidic Media». Inorganic Chemistry. 40 (4): 703–709. PMID 11225112. doi:10.1021/ic000793q
- ↑ Greenwood, Norman N.; Earnshaw, Alan (1997). Chemistry of the Elements (em inglês) 2ª ed. [S.l.]: Butterworth-Heinemann. ISBN 978-0-08-037941-8