Hexaboreto de lantânio
| Hexaboreto de lantânio Alerta sobre risco à saúde | |
|---|---|
| |

| |
| Outros nomes | Boreto de lantânio |
| Identificadores | |
| Número CAS | |
| Propriedades | |
| Fórmula molecular | LaB6 |
| Massa molar | 203.78 g/mol |
| Aparência | violeta púrpura intenso |
| Densidade | 2,61 g·cm-3 (20 °C)[1] |
| Ponto de fusão |
2210 °C[1] |
| Solubilidade em água | insolúvel[1] |
| Estrutura | |
| Estrutura cristalina | Cúbico |
| Grupo de espaço | Pm3m ; Oh |
| Página de dados suplementares | |
| Estrutura e propriedades | n, εr, etc. |
| Dados termodinâmicos | Phase behaviour Solid, liquid, gas |
| Dados espectrais | UV, IV, RMN, EM |
| Exceto onde denotado, os dados referem-se a materiais sob condições normais de temperatura e pressão Referências e avisos gerais sobre esta caixa. Alerta sobre risco à saúde. | |


Hexaboreto de lantânio (LaB6, também chamado boreto de lantânio e LaB) é um composto químico inorgânico, um boreto do lantânio. É um material cerâmico refratário que tem um ponto de fusão de 2210 °C, e é insolúvel em água e ácido clorídrico. Ele tem uma baixa função trabalho e uma das mais altas emissividades de elétrons conhecidas, sendo estável no vácuo. Amostras estequiometricas são coloridas de um violeta-púrpura intenso, enquanto aquelas ricas em boro (acima de LaB6.07) são azuis. Borbardeamento por íons altera sua cor de púrpura para verde esmeralda.[2]
O principal uso do hexaboreto de lantânio é em cátodos quentes, quer como um cristal único ou como revestimento depositado por deposição física de vapor. Hexaboretos, tais como o hexaboreto de lantânio (LaB6) e hexaboreto de cério (CeB6), tem baixas funções de trabalho, aproximadamente 2,5 eV. Eles também são pouco resistentes ao envenenamento do cátodo. Cátodos de hexaboreto de cério tem uma menor taxa de evaporação a 1700 K que o hexaboreto de lantânio, mas eles tornam-se iguais a temperaturas acima de 1850 K.[3] Cátodos de hexaboreto de cério tem uma e meia vez o tempo de vida dos de hexaboreto de lantânio, devido à anterior maior resistência à contaminação por carbono. Cátodos de hexaboreto são aproximadamente dez vezes mais "brilhantes" que cátodos de tungstênio, e tem 10-15 vezes mais longo tempo de vida. Dispositivos e técnicas nas quais cátodos de hexaboreto são usados incluem microscópios eletrônicos, tubos de microondas, litografia por elétrons, soldagem por feixe de elétrons, tubos de raios X, e laser de elétrons livres. Hexaboreto de lantânio lentamente evapora dos cátodos aquecidos e forma depósitos sobre os cilindroS de Wehnelt e aberturas. LaB6 é também usado como um padrão de tamanho/tensão em difração de pó por raio X para calibrar o alargamento instrumental dos picos de difração.[4]
LaB6 é um supercondutor com uma temperatura de transição relativamente baixa de 0,45 K. [5]
Estrutura
[editar | editar código-fonte]
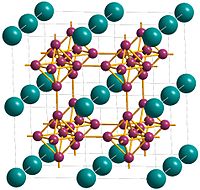
Hexaboreto de lantânio é um composto cerâmico pertencente ao grupo dos boretos. Apresenta uma estrutura relativamente incomum, na qual íons La3+ emparelham-se com clusters octaédricos aniônicos formados por seis átomos de boro (hexaboreto). Essa entidade é um polímero tridimensional, no qual cada boro do vértice de um octaedro se liga a um boro de outro octaedro, formando uma estrutura tridimensional. Cada octaedro de seis boros carrega uma carga negativa de -2. Um elétron livre está presente na estrutura para anular a terceira carga positiva do lantânio.
As ligações químicas entre os cátions de lantânio e os ânions hexaboreto poliméricos são ligações iônicas. Também há ligação metálica entre os íons de lantânio por meio dos elétrons livres. As ligações entre os boros de um octaedro e o octaedro vizinho são ligações covalentes simples B–B, enquanto as ligações entre os boros dentro de cada octaedro são um híbrido de ressonância entre ligações covalentes simples e ligações tricentradas com 2 elétrons. Este composto possui, portanto, os três tipos básicos de ligação química (iônica, covalente e metálica) simultaneamente.[6]
Referências
[editar | editar código-fonte]- ↑ a b c Base de dados Hexaboreto de lantânio por AlfaAesar, consultado em 9. Februar 2010 .
- ↑ T. Lundström "Structure, defects and properties of some refractory borides" Pure & Appl. Chem. 57(10) 1383 (1985) free download.
- ↑ «Comparing Lanthanum Hexaboride (LaB6) and Cerium Hexaboride (CeB6) Cathodes». Consultado em 5 de maio de 2009
- ↑ C. T. Chantler, C. Q. Tran, and D. J. Cookson (2004). «Precise measurement of the lattice spacing of LaB6 standard powder by the x-ray extended range technique using synchrotron radiation». Phys. Rev. A. 69: 042101. doi:10.1103/PhysRevA.69.042101
- ↑ G. Schell, H. Winter, H. Rietschel, and F. Gompf (1982). «Electronic structure and superconductivity in metal hexaborides». Phys. Rev. B. 25: 1589. doi:10.1103/PhysRevB.25.1589
- ↑ https://www.researchgate.net/figure/The-crystal-structure-of-Lanthanum-hexaboride-Two-unit-cells-are-shown-in-order-to_fig1_253260780
