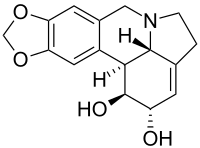
Licorina
| Licorina Alerta sobre risco à saúde | |
|---|---|
| |
| Nome IUPAC | 1,2,4,5,12b,12c-Hexahydro-7H-[1,3]dioxolo[4,5-j]pyrrolo[3,2,1-de]phenanthridine-1,2-diol |
| Outros nomes | Galanthidine, Amarylline, Narcissine, Licorine, Belamarine |
| Identificadores | |
| Número CAS | |
| PubChem | |
| ChemSpider | |
| ChEBI | |
| SMILES |
|
| InChI | 1/C16H17NO4/c18-11-3-8-1-2-17-6-9-4-12-13(21-7-20-12)5-10(9)14(15(8)17)16(11)19/h3-5,11,14-16,18-19H,1-2,6-7H2/t11-,14-,15+,16+/m0/s1
|
| Propriedades | |
| Fórmula química | C16H17NO4 |
| Massa molar | 287.29 g mol-1 |
| Página de dados suplementares | |
| Estrutura e propriedades | n, εr, etc. |
| Dados termodinâmicos | Phase behaviour Solid, liquid, gas |
| Dados espectrais | UV, IV, RMN, EM |
| Exceto onde denotado, os dados referem-se a materiais sob condições normais de temperatura e pressão Referências e avisos gerais sobre esta caixa. Alerta sobre risco à saúde. | |
Licorina é um alcaloide cristalino tóxico encontrado em várias espécies de plantas, tais como Clivia miniata, Amaryllis belladonna e diversas espécies dos géneros Lycoris e Narcissus. O composto é altamento venenoso, por vezes letal se consumido em grande quantidade. Os sintomas de intoxicação por licorina são vómitos, diarreia e convulsões.[1] Apesar dos riscos inerentes, o composto é por vezes utilizada medicinalmente, razão pela qual a popular Clivia miniata é colhida.
Descrição
[editar | editar código-fonte]Inibe a síntese de proteínas,[2] e poderá inibir a biossíntese de ácido ascórbico, apesar dos estudos existentes acerca deste último efeito serem controversos e inconclusivos.
Na actualidade, este alcaloide tem despertado o interess no estudo de algumas leveduras, o principal grupo de organismos sobre os quais tem sido ensaiado.[3]
Observou-se que a licorina possui também propriedades anti-inflamatórias[4] e antitumoral,[5] e mostra ter actividade contra a malária[6] e certos vírus, como o da pólio[7] e o vírus causador do SARS.[8]
A licorina também pode ser encontrada nos bolbos de narciso, os quais são frequentemente confundidos com cebolas.
Referências
- ↑ «Lycorine, definition at mercksource.com» (em inglês)
- ↑ Vrijsen R, Vanden Berghe DA, Vlietinck AJ, Boeyé A (1986). «Lycorine: a eukaryotic termination inhibitor?». J. Biol. Chem. 261 (2): 505–7. PMID 3001065
- ↑ Garuccio I, Arrigoni O (1989). «[Various sensitivities of yeasts to lycorine]». Boll. Soc. Ital. Biol. Sper. (em italiano). 65 (6): 501–8. PMID 2611011
- ↑ Yui S, Mikami M, Mimaki Y, Sashida Y, Yamazaki M. (2001). «Inhibition effect of Amaryllidaceae alkaloids, lycorine and lycoricidinol on macrophage TNF-alpha production (Japans)». Yakugaku Zasshi. 121 (2): 167-71. PMID 11218731
- ↑ Liu J, Li Y, Tang LJ, Zhang GP, Hu WX. (2007). «Treatment of lycorine on SCID mice model with human APL cells.». Biomed Pharmacother. 61 (4): 229-34. PMID 17336028
- ↑ Likhitwitayawuid K, Angerhofer CK, Chai H, Pezzuto JM, Cordell GA, Ruangrungsi N. (1993). «Cytotoxic and antimalarial alkaloids from the bulbs of Crinum amabile.». J Nat Prod. 56 (8): 1331-38. PMID 8229016
- ↑ Hwang YC, Chu JJ, Yang PL, Chen W, Yates MV. (2008). «Rapid identification of inhibitors that interfere with poliovirus replication using a cell-based assay.». Antiviral Res. 77 (3): 232-6. PMID 18243348
- ↑ Li SY, Chen C, Zhang HQ, Guo HY, Wang H, Wang L, Zhang X, Hua SN, Yu J, Xiao PG, Li RS, Tan X. (2005). «Identification of natural compounds with antiviral activities against SARS-associated coronavirus.». Antiviral Res. 67 (1): 18-23. PMID 15885816
