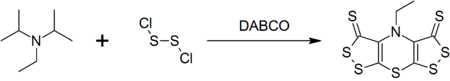N,N-Di-isopropiletilamina
| N,N-Di-isopropiletilamina Alerta sobre risco à saúde | |
|---|---|

| |

| |
| Outros nomes | Etildi(propan-2-il)amina N-etil-N-isopropilpropan-2-amina |
| Identificadores | |
| Número CAS | |
| PubChem | |
| Número EINECS | |
| ChemSpider | |
| MeSH | |
| SMILES |
|
| Propriedades | |
| Fórmula química | C8H19N |
| Massa molar | 129.24 g mol-1 |
| Aparência | Líquido incolor |
| Odor | Similar ao de peixe, amoniacal |
| Densidade | 0.742 g mL−1 |
| Ponto de fusão |
-50 a -46 °C |
| Ponto de ebulição |
127 °C, 399.7 K, 260 °F |
| Solubilidade em água | 4.01 g/L (a 20 °C) |
| Pressão de vapor | 4.1 kPa (a 37.70 °C) |
| Índice de refracção (nD) | 1.414 |
| Riscos associados | |
| Limites de explosividade | 0.7–6.3% |
| LD50 | 200–500 mg kg−1 (oral, rat) |
| Página de dados suplementares | |
| Estrutura e propriedades | n, εr, etc. |
| Dados termodinâmicos | Phase behaviour Solid, liquid, gas |
| Dados espectrais | UV, IV, RMN, EM |
| Exceto onde denotado, os dados referem-se a materiais sob condições normais de temperatura e pressão Referências e avisos gerais sobre esta caixa. Alerta sobre risco à saúde. | |
N,N-Di-isopropiletilamina, ou base de Hünig, DIPEA ou DIEA, é um composto orgânico e uma amina. É usada em química orgânica como uma base. Devido ao átomo de nitrogênio ser protegido pelos dois grupos isopropil e um grupo etilo somente um próton é pequena o suficiente para caber facilmente. Como a 2,2,6,6-tetrametilpiperidina, este composto é uma boa base mas um nucleófilo fraco, o que o faz ser um reagente orgânico útil.[1] A base de Hünig é nomeada em homenagem ao químico alemão Siegfried Hünig. Apresenta-se como um líquido incolor.
Base de Hünig é comercialmente disponível. É tradicionalmente preparado pela alquilação de di-isopropilamina com sulfato de dietila.[2] Se necessário, o composto pode ser purificado por destilação com hidróxido de potássio.
Reações
[editar | editar código-fonte]Base não nucleofílica
[editar | editar código-fonte]A base de Hünig tem sido investigada por seu uso como um reagente seletivo na alquilação de aminas secundárias a aminas terciárias por haletos de aquila. Esta reação orgânica é frequentemente dificultada por uma reação de quaternização ao sal quaternário de amônio mas esta reação lateral está ausente quando a base de Hünig está presente.[3]]
Síntese de escorpionina
[editar | editar código-fonte]A base de Hünig forma um composto complexo heterocíclico chamado escorpionina por uma reação com dicloreto de dienxofre catalizado por DABCO em uma síntese em uma única etapa (one pot).[4]
Referências
- ↑ Sorgi, K. L. (2001). «Diisopropylethylamine». Encyclopedia of Reagents for Organic Synthesis. doi:10.1002/047084289X.rd254
- ↑ Hünig, S.; Kiessel, M. (1958). «Spezifische Protonenacceptoren als Hilfsbasen bei Alkylierungs- und Dehydrohalogenierungsreaktionen». Chemische Berichte. 91 (2): 380–392. doi:10.1002/cber.19580910223
- ↑ Moore, J. L.; Taylor, S. M.; Soloshonok, V. A. (2005). «An efficient and operationally convenient general synthesis of tertiary amines by direct alkylation of secondary amines with alkyl halides in the presence of Huenig's base». Arkivoc. 2005 (part vi): 287–292. EJ-1549C. Consultado em 6 de outubro de 2017. Arquivado do original em 4 de março de 2008
- ↑ Rees, W.; Marcos, C. F.; Polo, C.; Torroba, T.; Rakitin O. A. (1997). «From Hünig's Base to Bis([1,2]dithiolo)-[1,4]thiazines in One Pot: The Fast Route to Highly Sulfurated Heterocycles». Angewandte Chemie International Edition. 36 (3): 281–283. doi:10.1002/anie.199702811