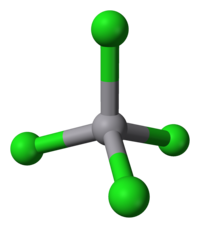
Cloreto de vanádio(IV)
Cloreto de vanádio(IV) ou Tetracloreto de vanádio é um composto químico inorgânico de fórmula VCl4. Em condições normais de temperatura e pressão, apresenta-se na forma de um líquido de coloração vermelho intenso. É um reagente bastante útil na preparação de outros compostos de vanádio.
Síntese e propriedades básicas
[editar | editar código-fonte]Com um elétron de valência a mais do que o composto diamagnético TiCl4, o VCl4 é um líquido paramagnético. Esse é um dos poucos compostos líquidos paramagnéticos que nas CNTP.
Tetracloreto de vanádio é preparado pela cloração do vanádio metálico. VCl5 não é formado no processo pois o Cl2 não possui força suficiente para atacar o VCl4. Em contraste, os análogos mais pesados NbCl5 and TaCl5 e não formam agente oxidantes.
Aplicações
[editar | editar código-fonte]VCl4 é um catalisador para polimerização de alcenos, particularmente útil na indústria da borracha. Uma tecnologia subjacente é relacionada à catálise Ziegler-Natta, que envolvem alquilas de vanádio como compostos intermediários.
Química Orgânica
[editar | editar código-fonte]Na sintese orgânica, VCl4 é utulizado para acoplar fenóis. Por exemplo, converte o fenol em 4,4'-bisfenol.[1] VCl
3 é reduzido no processo.
- 2 C6H5OH + 2 VCl4 → HOC6H4–C6H4OH + 2 VCl3 + 2 HCl
Essa reação realça a habilidade de oxidação do VCl4.
Segurança
[editar | editar código-fonte]VCl4 é volátil, oxidante forte e que hidrolisa rapidamente em água formando HCl.
Referências
[editar | editar código-fonte]- ↑ Calderazzo, F.; Maichle-Mossmer, C.; Pampaloni, G. and Strähle, J. (1993). «Low-temperature Syntheses of Vanadium(III) and Molybdenum(IV) Bromides by Halide Exchange». Dalton Transactions: 655–8. doi:10.1039/DT9930000655