Diclorofenol-indofenol
| Diclorofenol-indofenol Alerta sobre risco à saúde | |
|---|---|
| |

|

|
| Outros nomes | Dicloroindofenol (); 2,6-Diclorofenolindofenol; |
| Identificadores | |
| Abreviação | DCPIP, DCIP, DPIP |
| Número CAS | |
| PubChem | |
| ChemSpider | |
| KEGG | |
| ChEBI | |
| SMILES |
|
| InChI | 1/C12H7Cl2NO2/c13-10-5-8(6-11(14)12(10)17)15-7-1-3-9(16)4-2-7/h1-6,16H
|
| Propriedades | |
| Fórmula química | C12H7Cl2NO2 |
| Massa molar | 268.08 g mol-1 |
| Página de dados suplementares | |
| Estrutura e propriedades | n, εr, etc. |
| Dados termodinâmicos | Phase behaviour Solid, liquid, gas |
| Dados espectrais | UV, IV, RMN, EM |
| Exceto onde denotado, os dados referem-se a materiais sob condições normais de temperatura e pressão Referências e avisos gerais sobre esta caixa. Alerta sobre risco à saúde. | |
2,6-Diclorofenol-indofenol (DCPIP, DCIP ou DPIP nas siglas em língua inglesa para Di Chloro Phenol Indo Phenol) é um composto químico usado como corante redox. Quando oxidado, DCPIP é azul com absorção máxima a 600nm; quando reduzido, DCPIP é incolor.
Estrutura[editar | editar código-fonte]

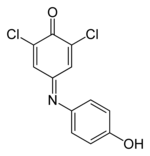
O diclorofenol-indofenol é um derivado clorado do indofenol, contendo dois átomos de cloro ligados a um dos anéis da estrutura em posições orto (2 e/ou 6) em relação aos átomos de oxigênio. É formado por dois anéis hexagonais de átomos de carbono ligados a um átomo de nitrogênio (que está na forma de uma imina), sendo um desses anéis um anel benzênico e o outro um anel quinoide, ambos possuindo átomos de oxigênio ligados em posições para (posição 4), diametralmente opostos ao átomo de nitrogênio. Um desses oxigênios, o do anel quinoide, liga-se por ligação dupla ao carbono 4 do anel, enquanto o outro, ligado ao carbono 4 do anel benzênico, está presente na forma de um grupo -OH, constituindo um grupo fenol.
O DCPIP existe na forma de dois tautômeros interconversíveis: em um deles, os dois cloros estão ligados ao anel benzênico, e no outro, ao anel quinoide. O composto possui um leve caráter ácido, e uma vez desprotonado, o ânion resultante é estabilizado por ressonância, de forma que desaparece a diferença entre os dois tautômeros: o anel benzênico e o quinoide se misturam no híbrido de ressonância, adquirindo um caráter intermediário entre os dois tipos. Isso ajuda a deslocalizar a carga negativa por toda a estrutura, o que acentua seu caráter ácido. Esse ânion apresenta uma cor azul, enquanto a forma protonada é rosa pálida. O composto é disponível comercialmente como seu sal de sódio.[1]
DCPIP é um agente oxidante suave que tende a receber dois elétrons, uma característica proveniente das propriedades do anel quinoide, impulsionada pela sua tendência à aromatização[2] para formar um anel benzênico. Essa propriedade se torna mais acentuada em meio ácido, uma vez que a forma protonada carece do híbrido de ressonância entre os dois tipos de anéis, o que individualiza o anel quinoide e facilita sua redução.
Aplicações[editar | editar código-fonte]
O DCPIP pode ser usado para medir a taxa de fotossíntese. Ele faz parte da família de reagentes de Hill. Quando exposto à luz em um sistema fotossintético, o corante é descolorido por redução química. O DCPIP tem uma afinidade maior por elétrons do que a ferredoxina, e a cadeia transportadora de elétrons fotossintética pode reduzir o DCPIP como um substituto para o NADP+, que normalmente é o transportador de elétrons final na fotossíntese. À medida que o DCPIP é reduzido e se torna incolor, o aumento resultante na transmitância de luz pode ser medido usando um espectrofotômetro.
O DCPIP também pode ser usado como um indicador para vitamina C.[3][4] Se a vitamina C, que é um bom agente redutor, estiver presente, o corante azul, que se torna rosa em condições ácidas, é reduzido a um composto incolor pelo ácido ascórbico. Esta reação é uma reação redox: a vitamina C (ácido ascórbico) é oxidada a ácido deidroascórbico, e o DCPIP é reduzido ao composto incolor DCPIPH
2.
- DCPIP (azul) + H+ → DCPIPH (rosa)
- DCPIPH (rosa) + vitamina C → DCPIPH2 (incolor)
Nesta titulação, quando todo o ácido ascórbico na solução tiver sido usado, não haverá elétrons disponíveis para reduzir o DCPIPH e a solução permanecerá rosa devido ao DCPIPH. O ponto final é uma cor rosa que persiste por 10 segundos ou mais, se não houver ácido ascórbico suficiente para reduzir todo o DCPIPH. Experimentos farmacológicos sugerem que o DCPIP pode servir como um quimioterápico pró-oxidante direcionado a células cancerígenas humanas em um modelo animal de melanoma humano; a morte de células cancerígenas induzida por DCPIP ocorre pela depleção de glutationa intracelular e regulação positiva do estresse oxidativo.[5]
Veja também[editar | editar código-fonte]
Referências
- ↑ https://www.pro-analise.com.br/2-6-diclorofenolindofenol-dihidratado_1030280005-Merck?user=fox_proanalise
- ↑ https://www.researchgate.net/figure/Aromatization-using-quinone-based-oxidants_fig1_354438040
- ↑ VanderJagt DJ, Garry PJ, Hunt WC (junho de 1986). «Ascorbate in plasma as measured by liquid chromatography and by dichlorophenolindophenol colorimetry». Clin. Chem. 32 (6): 1004–6. PMID 3708799
- ↑ Design an investigation to compare the amount of vitamin C in different fruits and vegetables (em inglês), consultado em 18 de novembro de 2023
- ↑ Cabello CM, Bair WB, Bause AS, Wondrak GT (agosto de 2009). «Antimelanoma activity of the redox dye DCPIP (2,6-dichlorophenolindophenol) is antagonized by NQO1». Biochem. Pharmacol. 78 (4): 344–54. PMC 2742658
 . PMID 19394313. doi:10.1016/j.bcp.2009.04.016
. PMID 19394313. doi:10.1016/j.bcp.2009.04.016

