Indofenol
| Indofenol | |
|---|---|
 | |
 | |
 | |
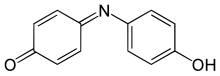
| Nome IUPAC | 4-(4-hidroxifenil)iminociclohexa-2,5-dien-1-ona |
| Outros nomes | Benzenona-indofenol, fenol-indofenol[1] |
| Identificadores | |
| Número CAS | |
| PubChem | |
| ChemSpider | |
| SMILES |
|
| InChI | 1/C12H9NO2/c14-11-5-1-9(2-6-11)13-10-3-7-12(15)8-4-10/h1-8,14H
|
| Propriedades | |
| Fórmula química | C12H9NO2 |
| Massa molar | 199.19 g mol-1 |
| Aparência | Pó azul-avermelhado.[1] |
| Ponto de fusão |
acima de 300 °C |
| Página de dados suplementares | |
| Estrutura e propriedades | n, εr, etc. |
| Dados termodinâmicos | Phase behaviour Solid, liquid, gas |
| Dados espectrais | UV, IV, RMN, EM |
| Exceto onde denotado, os dados referem-se a materiais sob condições normais de temperatura e pressão Referências e avisos gerais sobre esta caixa. Alerta sobre risco à saúde. | |
O indofenol é um composto orgânico com a fórmula O=C6H4=N–C6H4–OH. É um corante azul profundo, produto da reação de Berthelot, um teste comum para amônia. [2] O grupo indofenol, com vários substituintes no lugar de –OH e várias substituições no anel, é encontrado em muitos corantes usados em tinturas de cabelo e têxteis. [3] A molécula é solúvel em etanol e NaOH 1M [2], embora seja ligeiramente solúvel em água.
O indofenol é utilizado em tinturas capilares, lubrificantes, materiais redox, displays de cristal líquido, células de combustível e polimento químico-mecânico . É um poluente ambiental e é tóxico para os peixes. [1][4]
Síntese
[editar | editar código-fonte]O indofenol pode ser produzido a partir da reação entre a amônia e o fenol em meio básico na presença de hipoclorito de sódio como agente oxidante. A partir da mistura de compostos incolores, uma cor azul rapidamente se desenvolve e se torna cada vez mais intensa, denunciando a formação do produto. Nitroprussiato de sódio costuma ser usado como catalisador para essa reação. [5][6]
O mecanismo da reação envolve a formação de cloramina a partir da reação química entre a amônia e o hipoclorito de sódio, a qual é um composto altamente eletrofílico e ataca o anel benzênico do fenol, em especial em posições mais ricas em densidade eletrônica, como a posição 4 (para), formando o composto para-aminofenol com liberação de HCl que é rapidamente neutralizado pelo meio básico. [7] O para-aminofenol também é atacado pelo hipoclorito formando o intermediário para-cloraminofenol, que irá reagir com outra molécula de fenol (semelhante à cloramina na primeira etapa) resultando no composto bis(4-hidroxifenil)amina, que finalmente é oxidado por um terceiro íon hipoclorito para formar o indofenol.[8]

Alternativamente, esse composto pode ser formado na reação do fenol com paracetamol e hipoclorito em meio básico. A base hidrolisa o paracetamol (4-acetamidofenol) produzindo acetato e o para-aminofenol, que é convertido no composto cloraminado pelo hipoclorito, reage com o fenol e é em seguida oxidado por mais hipoclorito dando o indofenol.[9]
Outra reação semelhante pode ocorrer entre o paracetamol e um salicilato ou derivado (como a aspirina) [10]em meio fortemente básico, na presença de hipoclorito ou outro oxidante, inclusive o oxigênio do ar. O resultado dessa reação é um corante azul relacionado, o 2-carboxi-indofenol, que se diferencia do indofenol original por possuir um grupo carboxila (–COOH) ligado a um dos anéis, ao lado do grupo –OH. [11]

Teste de Berthelot
[editar | editar código-fonte]No teste de Berthelot (1859), uma amostra suspeita de conter amônia é tratada com hipoclorito de sódio e fenol. A formação do indofenol é usada para determinar amônia e paracetamol por espectrofotometria. [12][13]Outros fenóis podem ser usados. O diclorofenol-indofenol (DCPIP), um derivado clorado de indofenol, é frequentemente usado para determinar a presença de vitamina C (ácido ascórbico). [13]
Reações
[editar | editar código-fonte]O indofenol existe em solução em duas formas tautoméricas, embora idênticas entre si, que caracterizam a reatividade da molécula. O indofenol é um composto que funciona como um indicador ácido-base: ele apresenta sua cor azul-índigo característica em pH básico (na forma de seu sal indofenato), mas altera sua cor para alaranjado em meio ácido (devido à protonação de seu grupo amina).[14]


O indofenol também é um agente oxidante suave: na presença de alguns agentes redutores, como glicose em meio fortemente básico ou vitamina C (ácido ascórbico), entre outros, ele pode ser reduzido recebendo dois hidrogênios para formar o composto bis(4-hidroxifenil)amina, também chamado leuco-indofenol, um composto de cor rosa-pêssego muito pálida. A adição de um oxidante (inclusive o gás oxigênio) reoxida esse composto de volta ao indofenol, restaurando a cor original do composto (azul em meio básico e alaranjado em meio ácido). Devido à mudança de cor de acordo com seu estado de oxidação, o indofenol e seus derivados são úteis como indicadores redox.[15]

O indofenol também pode sofrer reação de halogenação na presença de halogênios como o cloro ou o bromo, mesmo sem o auxílio de catalisadores. Essa reação produz geralmente derivados cujos átomos de halogênio substituem os hidrogênios ligados aos carbonos dos anéis que se encontram vizinhos aos oxigênios (posições orto). Um derivado clorado importante, o diclorofenol-indofenol (DCPIP), é um reagente analítico muito utilizado na detecção de vitamina C.[13]
Referências
- ↑ a b c Erro de citação: Etiqueta
<ref>inválida; não foi fornecido texto para as refs de nomeb1 - ↑ Patton, Charles J.; Crouch, S. R. (1977). «Spectrophotometric and kinetics investigation of the Berthelot reaction for the determination of ammonia». Analytical Chemistry. 49 (3): 464–469. doi:10.1021/ac50011a034
- ↑ Horst Berneth (2002). «Azine Dyes». Ullmann's Encyclopedia of Industrial Chemistry. Weinheim: Wiley-VCH. ISBN 978-3527306732. doi:10.1002/14356007.a03_213.pub2
- ↑ «Indophenol I5763». 500-85-6. Consultado em 11 de junho de 2020
- ↑ https://journals.sagepub.com/doi/pdf/10.1177/000456327801500164?__cf_chl_tk=GNPwms48z3I0v6yVt1o9Pd6olOKwtc94ghkTqNor.hQ-1719532688-0.0.1.1-4265
- ↑ https://www.sciencedirect.com/science/article/abs/pii/0039914089801055
- ↑ https://www.researchgate.net/figure/The-reaction-mechanism-proposed-for-the-Berthelot-reaction-consists-of-three-steps-i_fig1_7040736#:~:text=Jeremy%20P%20Walker-,The%20reaction%20mechanism%20proposed%20for%20the%20Berthelot%20reaction%20consists%20of,phenol%20to%20form%20an%20indophenol.
- ↑ https://www.researchgate.net/figure/The-reaction-mechanism-proposed-for-the-Berthelot-reaction-consists-of-three-steps-i_fig1_7040736
- ↑ https://pubmed.ncbi.nlm.nih.gov/34936709/
- ↑ https://iopscience.iop.org/article/10.1149/2754-2734/ac6a68
- ↑ a b https://recima21.com.br/index.php/recima21/article/download/2797/1993/17605
- ↑ Tsuboi, T.; Hirano, Y.; Shibata, Y.; Motomizu, S. (2002). «Sensitivity improvement of ammonia determination based on flow-injection indophenol spectrophotometry with manganese(II) ion as a catalyst and analysis of exhaust gas of thermal power plant». Analytical Sciences. 18 (10): 1141–4. PMID 12400662
- ↑ a b c Hughes, David Emlyn (1983). «Titrimetric Determination of Ascorbic Acid with 2,6-Dichlorophenol Indophenol in Commercial Liquid Diets». Journal of Pharmaceutical Sciences. 72 (2): 126–129. doi:10.1002/jps.2600720208
- ↑ (em inglês)http://books.google.it/books?id=EzDbTL9Oah0C&pg=PA196&lpg=PA196&dq=indophenol+pH+indicator&source=bl&ots=Nc--0pEPsb&sig=Q9mNo_IvSqv5dZBzevB5GCjWCQY&hl=it&sa=X&ei=Zi8HU4DFFaaQ4gThuIDwDQ&ved=0CFoQ6AEwAw#v=onepage&q=indophenol%20pH%20indicator&f=false Parâmetro desconhecido
|titolo=ignorado (|titulo=) sugerido (ajuda); Parâmetro desconhecido|editore=ignorado (ajuda); Em falta ou vazio|título=(ajuda) - ↑ https://www.sciencedirect.com/topics/chemistry/indophenol
